近日,我院龚涛课题组首次设计构建出具有细胞内高尔基体靶向作用的纳米递药系统并应用于肝纤维化的治疗,在大鼠模型上显示出治愈肝纤维化的作用。这一原创性研究成果近期发表在ACS Nano(IF=13.709)上(Golgi Apparatus-Targeted Chondroitin-Modified Nanomicelles Suppress Hepatic Stellate Cell Activation for the Management of Liver Fibrosis. ACS Nano, 2019, DOI: 10.1021/acsnano.8b06924)。
肝脏作为人体最重要的器官之一,与各种生物功能密切有关,肝纤维化是世界范围内发病率和死亡率都很高的一种疾病。肝纤维化发生在多种慢性肝脏疾病中,起因于细胞外基质蛋白的过度积累,包括I型和III型胶原蛋白、蛋白多糖、纤连蛋白和透明质酸。肝星状细胞(HSCs)的活化和细胞外基质蛋白的过度产生是疾病发生和发展过程中的关键因素,而HSCs中高尔基体负责修饰及运输这些纤维化相关蛋白。我们由此设想,通过破坏肝星状细胞高尔基体的结构阻断纤维化相关蛋白的修饰和运输,就有可能干扰肝纤维化的一个或多个步骤,从而抑制肝纤维化的发生和发展。
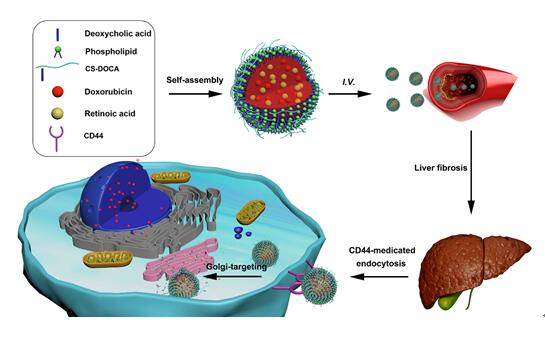
龚涛教授课题组首次发现一种可注射使用的生物材料--硫酸软骨素具有强烈的细胞内高尔基体靶向性,据此设计合成了硫酸软骨素(CS)衍生物,并将其应用于构建以CS为基础的纳米胶束,作为肝纤维化治疗的HSCs内高尔基体靶向特异性载体。课题组将阿霉素和反式维甲酸共载入CS胶束中,静脉注射后首先通过CS的CD44靶向性富集于肝脏HSCs中,然后通过GalNac-Ts介导靶向至细胞内高尔基体,随即胶束解体释放出药物,阿霉素由于其天然的趋核性到达细胞核干扰DNA的功能,诱导细胞凋亡,反式维甲酸留在高尔基体上破坏高尔基体结构,抑制胶原蛋白的合成。通过动物体内外实验研究证实了该递药系统对高尔基体的靶向性及其靶向机理,并在肝纤维化大鼠模型中显示出治愈肝纤维化的作用。CS胶束制备简单、毒性小、靶向效率高,具有广阔的应用前景和良好的临床转化潜力,是一种非常有前途的慢性肝病靶向治疗递送系统。
该工作得到了国家自然科学基金(81690261和81673359)的资助,文章的第一作者是金沙威尼斯欢乐娱人城2016级博士研究生罗静雯同学,通讯作者是龚涛教授。
来源:科研科 编辑:金沙威尼斯欢乐娱人城
